Estados Unidos prevé comenzar a vacunar contra la covid-19 a niños de 5 a 11 años a partir de noviembre, dijo el miércoles el gobierno de Joe Biden, una medida que hará que 28 millones de personas más puedan ser inmunizadas en ese país.
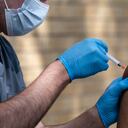
“Nuestros esfuerzos de planificación significan que estaremos preparados para comenzar a aplicar vacunas en los días posteriores a una recomendación final de los Centros para el Control y la Prevención de Enfermedades (CDC)”, señaló la Casa Blanca, aludiendo a la principal agencia federal de salud pública del país.
La farmacéutica Pfizer solicitó autorización para aplicar su vacuna anticovid en este grupo de edad a principios de este mes y la cuestión será debatida por dos paneles de expertos.

El primero, convocado por el regulador estadounidense de medicamentos FDA, se reunirá la próxima semana, y el segundo, convocado por los CDC, se reunirá el 2 y 3 de noviembre, y se espera que la agencia haga su recomendación poco después.
Durante un ensayo clínico, niños de 5 a 11 años recibieron dos dosis de 10 microgramos, en comparación con 30 microgramos para los grupos de mayor edad. Las inyecciones se administraron con 21 días de diferencia.
La vacuna desarrollada por la alianza Pfizer/BioNTech recibió aprobación total de la FDA para personas de 16 años en adelante y la FDA en mayo autorizó su uso de emergencia en niños de 12 a 15 años.
Los expertos dicen que vacunar a los niños es esencial para ayudar a lograr la inmunidad de la población contra la enfermedad.
Si bien los niños más pequeños tienen menos probabilidades de desarrollar casos graves de covid-19, aún pueden enfermarse y transmitir el virus al resto de la población.
Por otro lado, la confianza en las vacunas en Estados Unidos ha aumentado en los últimos meses. Hasta el miércoles, el 77,1% de la población actualmente elegible de 12 años en adelante había recibido una o más dosis de la vacuna anticovid.
Mezclar vacunas
El diario The Washington Post reveló el sentido de una de las decisiones que más expectativa ha generado recientemente en los Estados Unidos. El país está vacunando con la tercera dosis o la dosis de refuerzo a su población y ante esta nueva meta, saber si debía hacerse con la misma vacuna inicial o se podía utilizar una diferente era clave.

La FDA emitirá el miércoles un comunicado en el que según el diario dará la autorización de refuerzos para las vacunas Moderna y Johnson & Johnson. “Se espera que la FDA diga que las personas generalmente deberían ceñirse a la misma vacuna si es posible, pero permitir otras marcas de refuerzos, según dos funcionarios federales que hablaron bajo condición de anonimato porque no estaban autorizados a discutir el tema”, señala el periódico.
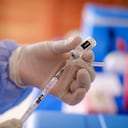
La decisión se toma luego de que se hicieran públicas varias investigaciones que evidenciaban la necesidad de reforzar a algunos vacunados. Las mayores dudas en Estados Unidos se tenían respecto a los vacunados con Johnson & Johnson (J&J). Un panel de expertos médicos estadounidenses de alto nivel aprobó por unanimidad recomendar la autorización de una segunda inyección de esta vacuna.
La decisión contribuirá a poner fin a una sensación de limbo para 15 millones de estadounidenses que recibieron la dosis única, pero que estaban preocupados de si sería suficiente para protegerlos, especialmente tras el aumento de la variante delta.
Los miembros del comité, convocados por la Administración de Alimentos y Medicamentos (FDA), coincidieron con la empresa farmacéutica en que las pruebas de seguridad y eficacia favorecían una segunda dosis de esta vacuna originalmente de una sola dosis.
Varios de los expertos independientes sugirieron que, aunque J&J había solicitado la autorización de un refuerzo, una segunda vacuna de J&J debería considerarse, de hecho, como una dosis “adicional” necesaria para lograr la vacunación completa. “Creo que esto francamente siempre fue una vacuna de dos dosis. Es difícil recomendarla como una vacuna de una sola dosis”, dijo Paul Offit, experto en vacunas del Hospital Infantil de Filadelfia.
Con información de AFP.
