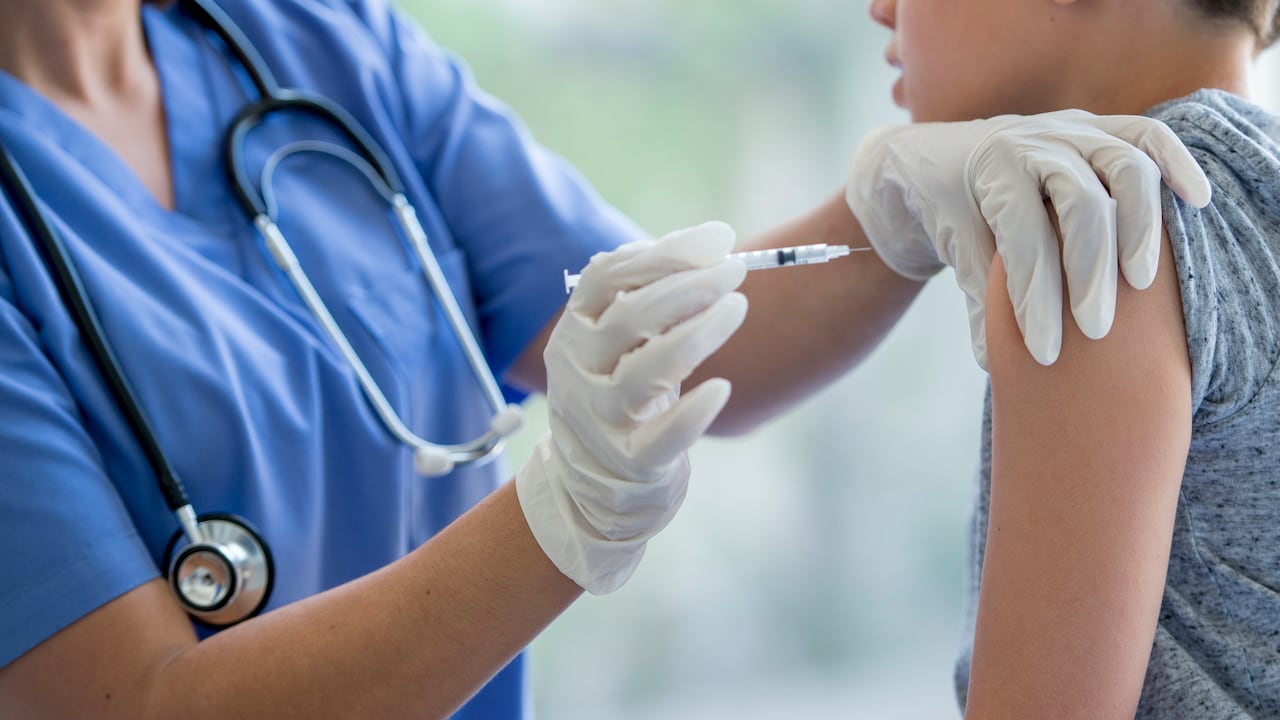
El Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) aprobó la modificación de la Autorización de Uso de Emergencia (ASUE) para la vacuna contra la covid-19 de Pfizer y BioNTech, permitiendo la inclusión de personas desde 12 años en adelante.
Debido a una solicitud que hizo el titular de la autorización, el Invima evaluó la evidencia y definió que la ampliación del grupo etario tiene un balance riesgo-beneficio favorable.
La Sala Especializada de Moléculas Nuevas, Nuevas Indicaciones y Medicamentos Biológicos de la Comisión Revisora del Invima, después de la decisión, resaltó que es fundamental que se adelanten estudios de efectividad, seguridad y uso en el contexto colombiano.
Por lo tanto, estableció la realización de estos en la población objeto de la solicitud de modificación de la ASUE, incluyendo la vigilancia activa de reacciones inflamatorias o de otra clase.
Por otra parte, cabe anotar que la ASUE está condicionada a los nuevos conocimientos que surjan en relación con la seguridad y eficacia de la vacuna, derivados de los estudios clínicos en curso y de la experiencia clínica que se va acumulando de su uso cotidiano.

Así, las nuevas indicaciones para la inoculación en la prevención de la covid-19 con esta vacuna, incluyen a los niños, niñas y adolescentes a partir de 12 años, proporcionándoles dos dosis administradas intramuscularmente y separadas entre sí por 21 días.
El anuncio del instituto se da dos semanas después de que el Ministerio de Salud anunciara la inclusión del grupo etario en el Plan Nacional de Vacunación, en dos etapas diferentes. Por una parte, las personas desde los 12 años con comorbilidades fueron sumadas al grupo de la etapa 3, mientras que las demás ahora son parte de la etapa 5.
Entre las comorbilidades listadas por la cartera están artritis reumatoide, lupus, vasculitis, diabetes, VIH, insuficiencia renal, cáncer, epoc, tuberculosis, asma, obesidad grados 1, 2 y 3, en lista de espera de trasplante de órganos o postrasplante, insuficiencia cardiaca, arritmia, enfermedad cerebrovascular, síndrome de Down, autismo, esquizofrenia, discapacidad intelectual, entre otras.
Todo esto fue incluido en el Decreto 630 de 2021, en el que también se añadieron las personas gestantes, aquellas mujeres que tuvieron un parto hasta dos meses antes y grupos adicionales a las etapas del plan.

En el acto administrativo dice que “las investigaciones que se han adelantado al respecto sugieren que la vacuna contra la covid-19 durante el embarazo es eficaz y segura, y dado el aumento de los riesgos asociados a la covid-19 durante la gestación, muchas mujeres embarazadas han decidido aceptar la vacunación sobre el supuesto que los beneficios superan los riesgos potenciales”.
No obstante, hasta el momento Pfizer no ha solicitado modificaciones de la autorización en ese sentido, por lo que, por ahora, las personas gestantes no recibirán la vacuna contra la covid-19.
Según el último corte, en Colombia se han aplicado 16.038.817 dosis de biológicos, de los cuales 5.381.189 corresponden a la segunda dosis. Es así como el país ya avanzó en un 15 % de la meta para el 31 de diciembre de 2021, de tener al 70 % de la población inmunizada contra la covid-19.