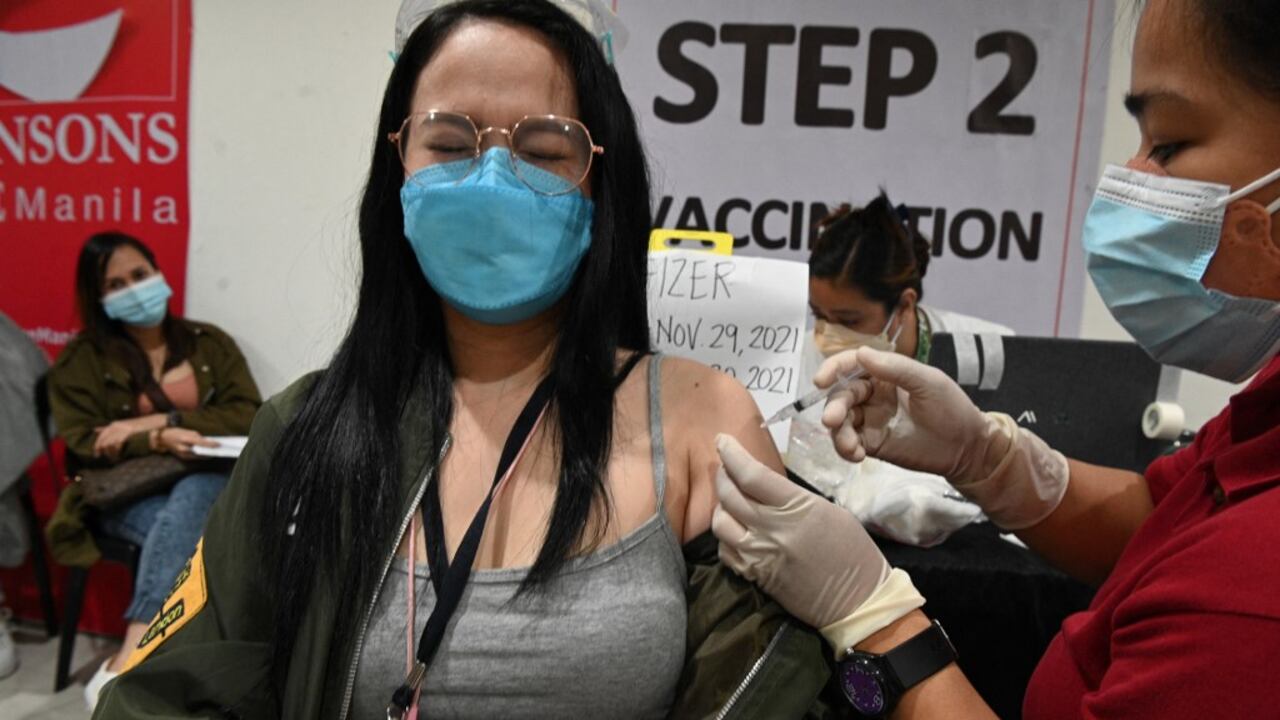
Mucho se ha hablado de la cantidad de vacunas que serán necesarias frente a la novedad de la covid 19, que puso a las empresas farmacéuticas a correr para desarrollar una primera vacuna. Luego las variantes del virus agudizaron el panorama.
Por el momento se sabe que con un esquema de una o dos vacunas y una dosis de refuerzo, el organismo puede estar protegido contra el SARS-CoV-2 y sus variantes por lo menos seis meses. Sin embargo, con la aparición de nuevas cepas y variantes la posibilidad de que esta inoculación sea constante es cada vez mayor.
De hecho, el CEO de la farmacéutica Pfizer, desarrolladora de uno de los biológicos contra la covid-19, Albert Bourla, le dijo a la cadena estadounidense CBS que sería necesario ponerse una cuarta dosis de refuerzo de su vacuna.
De acuerdo con las palabras de Bourla, a pesar de que las tres dosis que se contemplan hasta este momento brindarían al cuerpo la protección suficiente para detectar y eliminar el virus una vez una persona se ha contagiado, esta respuesta inmunológica podría no durar mucho.
Esta posibilidad de tener que aplicarse un biológico contra la covid-19 cada cierto tiempo obedece a las predicciones que han hecho algunos expertos de que esta se va a convertir en una enfermedad endémica, que se presentará por temporadas y climas, como la influenza o el dengue.
Según el director, su empresa ya puso en marcha las consultas con expertos para definir la viabilidad y seguridad de esta nueva dosis, que debería ser también aprobada por los organismos sanitarios de cada país luego de los ensayos pertinentes.

Así mismo, Pfizer afirmó encontrarse en constante comunicación y envío de información técnica con la Administradora de Alimentos y Medicamentos (FDA, por sus siglas en inglés) de Estados Unidos, quien deberá validar sus propuestas y permitir o negar el uso de esta nueva dosis que la farmacéutica planea implementar.
Por otro lado, la compañía compartió, a través de un comunicado, información que consigna el inicio de ensayos clínicos para la segunda y tercera fase de tratamientos en contra del coronavirus de la píldora Paxlovid, en niños de seis a 17 años.
Para dar resultados, el estudio tendrá en cuenta la eficacia del tratamiento antiviral en los menores que tienen signos de la covid-19 y su versión confirmada, pero que no están hospitalizados por infección grave.
La FDA ya había autorizado el uso de Paxlovid en sujetos de alto riesgo de contagio mayores a los 12 años de edad. Las indicaciones dicen que los pacientes deben pesar menos de 39 kilogramos, no obstante, esta decisión se tomó con base en ensayos de laboratorio donde las personas menores a los 17 años no estaban incluidas.
Según la empresa, los resultados de los ensayos mostraron que se redujo el riesgo de hospitalización y fallecimientos por covid-19 en un 89 % si es ingerido por adultos de alto riesgo que experimentan los primeros síntomas.
Conjuntamente, de acuerdo con información recopilada por el noticiero CNN, la autorización incluye a los mayores de 12 años según un modelo que muestra que tendría efectos similares en niños que en adultos. Así las cosas, Pfizer dice en su comunicado que el inicio de estos ensayos “brindará más apoyo para la recomendaciones de dosis en esta población, así como ampliar potencialmente la indicación a grupos de edad más jóvenes y de menor peso”.